原标题:椎间融合器注册技术审查指导原则
一、前言
椎间融合器作为骨科植入性医疗器械,是实现脊柱相邻椎间隙融合的主要植入物之一,其安全性和有效性直接影响相邻椎体骨性融合的效果。本指导原则旨在指导注册申请人对椎间融合器的产品注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
本指导原则系对椎间融合器的一般要求,申请人应依据具体产品特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
本指导原则是对申请人和审查人员的指导性文件,不涉及注册审批等行政事项,亦不作为法规强制执行,如有能满足相关法规要求的其他方法,也能够使用,但应提供详细的研究资料和验证资料。应在遵循相关法规和技术标准的前提下使用本指导原则。
本指导原则是在现行法规和标准体系以及当前认知水平下制定的,随着法规、标准体系的不断完善和科学技术的持续不断的发展,本指导原则相关联的内容也将适时做调整。
二、适用范围
本指导原则涵盖的产品系植入于椎间隙并联合脊柱内固定植入物使用的预定形的非可降解椎间融合器。椎体切除术(次全切及全切)中的椎体替代植入物,和特殊设计的产品如自稳定型、自撑开型、分体组合式、可吸收型等椎间融合器,可以参考本文的技术分析原理来制定适用的具体性能要求、试验方法、临床试验资料和使用说明书等相关注册资料。
三、技术审查要点
(一)注册单元的划分
椎间融合器临床预期用途较为统一,颈椎、胸腰椎产品可作为同一注册单元,不考虑微创、开放、前路、后路等脊柱减压手术术式区别。椎间融合器产品组件可包括主体、端盖(若有)、组件紧固螺钉(若有。不包括发挥脊柱内固定作用的椎弓根或椎体钉)等,各组件相互配套地使用于临床,且不同尺寸规格间配合关系较确定,故单一组件一般不作为独立注册单元进行申报。
(二)产品的研究资料
1. 产品的基本信息
(1)产品各型号规格、各组件、各关键部位的结构图和几何尺寸参数(包括允差)。例如终板接触面的弧度、倾角及咬合齿的高度,植骨区、涂层和显影区的边界及在融合器中位置,主体的长宽高度,端盖及紧固螺钉的直径,网孔结构的几何尺寸等。结构图应以产品CAD设计工程图为蓝本,从整体外观、各维度剖面及侧面、局部细节明确产品的设计特征。带多孔涂层的产品应运用ASTM F1854中的体视法明确其涂层厚度、孔隙率、平均截距。
(2)产品各组件及涂层的材料牌号及材料所符合的国家标准、行业标准、国际标准,材料牌号的描述应与其符合的标准一致。进口产品的材料牌号及符合标准同时不应超过原产国上市证明文件/说明书所批准/载明的范围。通常所涉及的材料相关标准包括但不限于:
GB/T 13810 外科植入物用钛及钛合金加工材
GB 23101.2 外科植入物羟基磷灰石 第2部分:羟基磷灰石涂层
YY/T 0660 外科植入物用聚醚醚酮(PEEK)聚合物的标准规范
YY/T 0966外科植入物 金属材料 纯钽
ASTM F 1609 可植入物材料用磷酸钙涂层的标准规范
ASTM F 1580 外科植入物涂层 钛及钛6铝4钒合金粉末
(3)各型号产品的具体适用部位。即各型号所对应的具体椎间隙节段,体现不同型号几何参数与不同节段椎体终板形状大小及椎间隙高度的匹配性。
2. 各型号规格的划分原则
正常的情况下除尺寸大小差异之外,外形相近的一系列产品归类为同一型号。外形的设计除与所使用节段的椎间隙几何特征相关外,还可能与植入融合器的手术入路相关。
3. 产品基体的力学性能研究资料
椎间融合器的力学性能对比测试方法较为统一,主要是按照YY/T0959及YY/T0960进行动静态力学测试,并按照两项行标出具详细的测试报告。以下为申报资料中需重点注意的部分内容。
按照YY/T0959进行的动静态测试中,受测样本的放置方式(例如单件斜置式)及与力加载轴的相对位置应模仿临床植入后产品与椎体的相对位置。静态力学测试中,样品量应不小于5件,载荷-位移曲线的参数应至少包括屈服位移、屈服载荷/扭矩、刚度、最大位移、最大载荷/扭矩的平均值和标准差;动态力学测试除了在生理盐水环境中测试并与常温空气中的测试进行对比,还应考虑模拟体液环境对测试的影响,尤其可能面临较大体液腐蚀和体内磨损的设计,如多孔疏松等比表面积较大的产品及多组件式产品,多组件式包括自稳定型融合器还应考虑组件间微动腐蚀的影响。最大载荷-循环次数失效趋势图中,数据组应不小于6组,最大疲劳载荷精度应小于静态最大载荷或扭矩的10%,使用回归分析方法应能建立载荷/扭矩与失效循环次数的关系,此关系曲线应为半对数曲线。轴向压缩、压缩剪切和扭转三种疲劳试验的初始失效和二次失效中的失效模式及组件形变情况均应记录,应明确失效(磨损、裂纹源及裂纹扩展情况)、失效区定位、组件结构的松弛及失效时的试验环境参数。从产品本质来讲,与失效有关的因素一般包括材料(例如不同刚度材料的组合)、载荷及其频率(例如颈椎扭转和腰椎压缩)、内部应力分布(例如应力集中区)、使用环境(例如腐蚀程度)、产品表面处理工艺及质量(例如喷砂后的残余应力及微裂纹源),等等。在选择最典型型号规格进行所申报产品代表性的力学测试时,例如所申报型号规格中最差情况的选择,应注意从以上方面做分析论证,包括烧结、增材制造、气相沉积等工艺制成的多孔疏松结构的产品。具有合理边界条件设置的有限元分析可能会帮助分析,对分析结果的论证中应考虑到实际临床使用中内固定器械、相邻椎体作用力及在体的骨整合过程(包括骨长入及骨长上)对弹性模量、应力分布等有限元分析模型参数的影响。
按照YY/T0960进行的试验中,应注意金属块及聚氨酯泡沫块条件下的载荷-位移曲线均应记录,应记录不少于5个融合器试验配置的失效模式、形变信息和相关数据。相关数据应包括屈服载荷的平均值和标准差、三项刚度数值——融合器刚度Kd、系统刚度Ks、聚氨酯泡沫块Kp。尤其Kp值对于评价融合器可能引起的椎体沉降较为关键。同样应注意论证所测试样品是能代表所申报产品的最典型型号规格。具有合理边界条件设置的有限元分析可能会帮助分析,对分析结果的论证中应考虑到实际临床使用中内固定器械、相邻椎体作用力及在体的骨整合过程(包括骨长入及骨长上)对弹性模量、应力分布等有限元分析模型参数的影响。
力学测试报告中应包含与已上市同品种产品数据的详细对比论证(对比测试或与既有实验数据对比),结合所植入节段的力学特点和周围的辅助保护措施,以明确测试结果可接受限(如疲劳极限、极限载荷、屈服载荷等)的判定依据。
4. 产品涂层力学测试研究资料
对于有涂层的产品,应按照ASTM F1044、F1147、F1160分别进行剪切试验、拉伸试验、剪切和弯曲剥脱疲劳试验。一般情况下,剪切强度应不低于20mpa,拉伸强度应不低于22mpa,疲劳试验应经历107正应力循环或持续到样件失效。剪切和拉伸试验报告中应注意包括最大、最小和平均失效载荷值,明确试样失效在涂层内部还是涂层与基体间还是两者均有;疲劳试验报告中除以上信息,还应注意包括R比(最小应力/最大应力)、试验频率、失效循环数、剪切疲劳试样尺寸、弯曲疲劳试验基准试样的基体表面粗糙度、涂层断裂位置。对于热喷涂于金属表面的金属涂层,还应注意按照ASTM F1978进行耐磨性能试验,明确2、5、10及100次循环累计质量损失的平均值及标准偏差,及研究过程中的磨损、掉色、脱落、腐蚀等发现。100个循环周期后,涂层质量损耗总值应小于65mg。
5. 产品生产工艺和过程控制
(1)详述产品的生产过程,提供生产工艺流程图。
(2)明确特殊过程和关键工艺,提供特殊过程的确认资料以及关键工艺的验证资料。例如表面涂层工艺过程中各类加工助剂的添加、去除和残留控制,包括闭孔中造孔剂。产品加工过程的常见助剂有切削液、冷却液、润滑剂、造孔剂、粘接剂、抛光剂、多孔支架材料、清洁剂等。对于有阳极氧化表面处理的钛及钛合金材质产品,尤其微弧阳极氧化,应明确氧化层引入的与基体材料不一致的新元素的质控措施,并通过适当的表面元素分析方法(如半定量定性分析)来评估该工艺的稳定性。
6. 灭菌确认
对于经辐照灭菌的产品,应明确辐照剂量并参考GB 18280、GB/T 19973等相关标准提供灭菌参数确定依据,至少包括初始平均生物负荷、VDmax剂量验证及最低剂量灭菌后无菌检测报告,完整的辐射灭菌确认报告还应包括产品及包装材料的选择、产品装载模式的确定、产品剂量分布图及确认过程中所负载的有抗力的微生物孢子信息;对于经环氧乙烷灭菌的产品,除依据GB 18279、GB 18281.2等相关标准提供关键参数的确定依据如预处理、处理、灭菌和通风4个过程中的温度、湿度、气体压力、EO浓度、灭菌作用时间等,完整的确认报告还应包括被灭菌品摆放方式与分隔形式、换气速度与气体压力、灭菌剂质量及体积、存活曲线法或部分阴性法鉴定的生物学性能等内容,此外还应提供终产品环氧乙烷残留量的质控验证数据;过氧化氢等离子体、气态过氧化氢等灭菌方法同样应提供关键灭菌参数的验证和确定依据包括灭菌时间、相对湿度、气体浓度、灭菌容积、生物指示剂灭菌动力学曲线、灭菌温度等。具有多孔结构和较大比表面积的产品,尤其应论证或验证灭菌工艺参数能够确保其无菌保证水平。
7. 无菌有效期验证
对于非灭菌产品,应明确推荐最终使用者采用的灭菌方法并提供验证资料。灭菌产品应参照《无源植入性医疗器械货架寿命申报资料指导原则》提供产品货架寿命尤其无菌效期的验证资料。鉴于本指导原则涵盖的产品为惰性材料产品,仅要求对其中包装系统的性能稳定性(至少包括包装完整性和包装强度)进行验证。对于不同包装、不同灭菌方式的产品应分别提供无菌效期验证资料。
8. 生物相容性评价
椎间融合器的生物相容性评价应按照GB/T16886.1中的系统方法框图及原国家食品药品监督管理局《关于印发医疗器械生物学评价和审查指南的通知》(国食药监械〔2007〕345号)中的审查要点进行生物学风险评价,在缺乏相关数据时,补充进行必要的生物相容性测试。
(三)产品的风险管理资料
根据YY/T 0316《医疗器械风险管理对医疗器械的应用》,充分识别椎间融合器的设计、原材料、生产加工、包装、灭菌、运输、贮存、使用等生命周期内各个环节的安全特征,从能量危害(若涉及)、生物学危害、环境危害、有关使用的危害、因功能失效、老化及存储不当引起的危害等方面,对产品进行全面的风险分析,并详述所采取的风险控制措施及验证结果,必要时应引用检测和评价性报告。对于多孔结构的产品,应考虑金属离子释放对人体的危害及剩余风险。对于有阳极氧化处理的钛及钛合金材质产品,应通过适当的生物学试验方法(至少包括细胞毒性测试)进行生物学危害的风险分析。
提供产品上市前对其风险管理活动进行全面评审所形成的风险管理报告,此报告旨在说明并承诺风险管理计划已被适当地实施,并经过验证后判定综合剩余风险是可接受的,已有恰当的方法获得产品相关、出厂后流通和临床应用的信息。
风险管理报告应包括风险分析、风险评价、风险控制等产品风险管理的相关资料,至少应包括产品安全特征清单、产品可预见的危害及危害分析清单(说明危害、可预见事件序列(即危害成因分析))、危害处境和可能发生的损害之间的关系、风险评价、风险控制措施以及剩余风险评价汇总表。
风险管理报告可参照附录《椎间融合器产品风险管理资料要求》进行编制。
(四)产品技术要求
应按照医疗器械产品技术要求编写指导原则进行编写。
对同一注册单元中存在多种型号和/或规格的产品,应明确各型号及各规格之间的所有区别,并附相应图示及数据表格对逐型号规格进行说明。
性能指标及检验方法的确定是技术要求的主要内容。性能指标的制定应参考相关国家标准/行业标准并结合具体产品的设计特性、预期用途和质量控制水平,且性能指标不应低于产品适用的强制性国家标准/行业标准,检验方法应优先考虑采用公认的或已颁布的标准检验方法,包括推荐性标准。若需要修改公认的标准检验方法以匹配产品的设计特点或具体使用方式,例如特殊工装及测试样品的制备方法,应在支持性资料中详细论证检验方法及测试结果可接受限的合理性。若原材料的化学成分、显微组织等技术要求经加工后仍适用于终产品,则可以列入性能指标。除非原材料的力学性能与成品的力学性能要求一致,否则产品技术要求中力学性能指标应针对终产品而不包括针对原材料的内容。建议椎间融合器的性能指标内容至少包括成品及涂层的静态力学性能测试,并且应与前述产品技术研究资料中相关内容一致。
(五)产品注册检验
注册检测的送检样品应符合抽样原则,在所有申报型号规格中具有代表性,包括力学性能方面的典型性,如YY/T 0959及YY/T 0960中颈椎、胸腰椎产品测试时位移偏移量、试验块高度、椎间盘高度等参数均有不同,颈、胸腰椎产品应分别选择典型型号进行力学性能的注册检测,应考虑产品(包括涂层)的力学性能最差情况。其他理化特性的典型性应考虑加工工艺与组件结构的复杂性。
(六)产品的临床评价
椎间融合器应按照《医疗器械临床评价技术指导原则》(以下简称《临床评价导则》)进行同品种产品的临床数据对比、分析、评价,并按照《临床评价导则》要求的项目和格式出具评价报告。按照《临床评价导则》附件4列明的分析评价路径,应首先选择通过所申报产品的非临床的实验室研究数据、所申报产品自身的临床历史数据(文献/经验/试验)进行评价,尤其对于仿制型和改进型产品的临床评价更有意义。事实上,同品种产品的筛选是在临床评价(包括非临床实验室研究数据的比对)过程中才逐步明确的,而不是完整临床评价之前能事先精确判定的。通过临床评价,最终所对比的同品种椎间融合器,相互之间存在一定的差异范围,却表现出实质相同的临床安全性及有效性,这就佐证了所申报产品在此差异范围内的设计变化带来的临床风险是可控的,安全有效性是可接受的。
(七)产品的临床试验
按照《临床评价导则》附件4的评价路径图,在与同品种的椎间融合器产品对比的临床评价之后或之前,都可能在中国境内进行所申报融合器的临床试验。前者是针对所申报产品与同品种产品对比出的差异性进行设计(包括评价指标的精细化)的临床试验,作为评价资料中自身临床数据的一部分,以证明差异之处不影响所申报融合器的安全有效;如果在通过本指导原则(六)部分中所述的针对临床历史数据的评价工作后,仍留有安全性/有效性盲点,且这些信息盲点必需开展新的临床试验、产生新的临床数据后方能完成风险评价,此时应当设计完成后者所述的临床试验,这可能是对既有的、针对差异性进行的临床试验的进一步研究(例如增加样本量或随访信息补充或挖掘),也可能针对所申报融合器进行了全新设计(如改变可降解产品主要评价指标为全身长期安全性指标而非常规的融合有效性指标),但绝不可能是对非临床实验室研究的替代,因为绝大部分风险控制通过非临床实验室数据能够更精确更有针对性地完成。这里要注意在所有科学合理的临床试验方案的建立之前,对已上市同品种产品的临床文献/经验/试验数据的评价是临床试验前工作的重要环节,应符合相应数据搜集和分析的科学方法并关注相应审评要点,即使申请人选择直接针对融合器整体进行临床试验(而非针对与同品种的差异性)来完成所申报产品的临床评价工作。产品的临床评价中的关注点同样适用于良好的临床试验,因为临床试验是临床评价数据的重要来源,而对临床历史数据的良好评价是高质量临床试验的基础。
1. 临床试验设计类型
申请人针对所申报产品进行的临床试验是临床研究类型中的纵向研究,但并非仅仅指随机平行对照的实验性研究,基于与产品设计表征相关的临床先验信息的分析,其他具有对照组的临床试验类型也应当考虑,从法规层面来讲,这些试验类型往往能体现出相应的伦理学及减轻试验负担等研究价值百科。例如历史对照试验(如目标值法等非同期历史对照)、部分随机试验(如试验组随机而对照组不随机等)、回顾性病例-对照研究等等,即使是平行分组对照试验,也不应局限于传统的配对平行设计,还应考虑试验组与对照组不等量分配的平行分组设计等研究类型。不同类型临床试验(临床研究)的数据质量及证据级别水平请参见相关教科书的阐述。虽然更先进的统计学原理能够帮助医疗器械的临床试验更加符合伦理且科学严谨地减少样本量或缩短临床试验时间,但需要强调的是所遵循的统计学原则及运用的统计计算方法应与不同试验设计类型相适应,以控制由于对随机性和盲态的破坏而造成的系统性偏倚。例如,贝叶斯分层模型基于前代及同类产品的先验信息与参数后验分布,在运用其原理进行适应性设计时,应严密注意引入的操作误差,包括选择偏倚、评价方法偏倚、治疗修订偏倚、治疗效应相应的可信区间错误、资料收集偏倚、患者纳入标准与分组变化、假设与统计矛盾等,对采取的应对措施应在方案中有相应的详细描述和论证,包括揭盲程序、独立数据管理委员会、独立的中心实验室、独立终点评价、对后验概率和预测分布的中期分析计划、所应用统计软件参数的设定等等。不过,经典的RCT试验的样本量计算和随访时点的设定及最终统计计算都比其他试验类型更简单,混杂因素控制得也最好,因而在技术审评中更容易得出结论。
统计学类型方面,具有对照组的试验常见的检验类型有非劣效、等效及优效。非劣效检验最为常用,但仍然需根据申报产品在主要评价指标方面预期所具有及宣称的有效性及安全性进行合理选择,否则一味地减少样本量或减轻时间等试验成本,将可能出现试验结果与方案设定的假设检验及参数不一致,引发进一步临床试验,例如方案中非劣效界值设定较大但两组试验结果均为100%,甚至试验组大大优于对照组,将可能挑战试验对假阳性的控制,或者挑战方案设定依据与试验执行之间的一致性,至少需要运用精确概率法对组间差异的点估计及可信区间做出计算,并严格考察实验设计的灵敏度。事实上如果在非劣效界值的论证中严格秉持高质量文献数据分析的原则,并确保与试验执行内容的一致性,则可确保假设检验的合理前提。
以下内容以经典频率学派的平行对照试验类型为例。
2. 临床评价指标
评价指标(观察终点)应从安全性与有效性两方面设定,有效性指标分主要评价指标与次要评价指标。
(1)主要评价指标
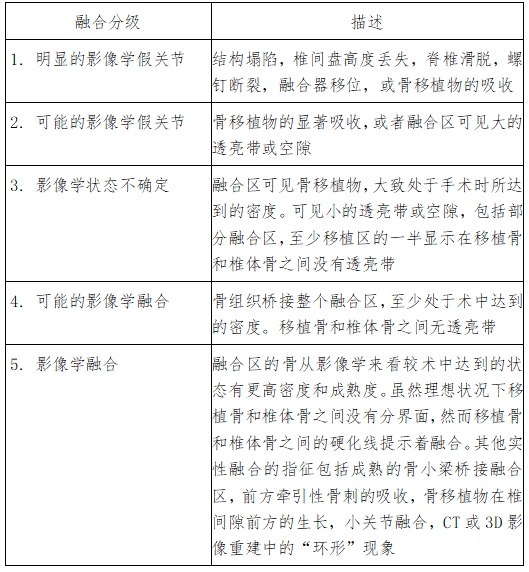
椎间融合器临床试验应以影像学终点为主要评价指标,观察椎间隙融合和融合器稳定性,即通过X线和CT三维重建来静态观察终板之间的骨小梁衔接,X线动力位观察包括椎间平移运动与屈伸角度变化,以构成联合指标。该联合指标对椎间融合的判定标准一般是分级式评价标准,按优良中可差分为若干等级。骨融合的静态影像学评定标准众多,临床试验方案中应明确表述。例如经典的Brantigan和Steffee提出的评定标准。需要注意的是,在该标准中须将第4、5级别合并统计出病例组的融合率,方为临床试验中通常使用的病例组的“优良率”或“有效率”所指的静态影像学信息。
表1 Brantigan和Steffee提出的融合结果
影像学分级(和描述)
融合区的骨从影像学来看较术中达到的状态有更高密度和成熟度。虽然理想状况下移植骨和椎体骨之间没有分界面,然而移植骨和椎体骨之间的硬化线提示着融合。其他实性融合的指征包括成熟的骨小梁桥接融合区,前方牵引性骨刺的吸收,骨移植物在椎间隙前方的生长,小关节融合,CT或3D影像重建中的“环形”现象
鉴于联合终点考虑静态融合度、椎间活动度等多个终点,应注意根据高质量权威文献制定联合量表,以确保最终设定的病患评定标准(治疗有效率的优良等级划分)的信度、效度、灵敏度、统一性。
值得注意的是,若临床试验方案设定的随访终点时辅助的内固定器械仍未取出,则椎间平移运动应为0mm,屈伸角度变化<2°,此类临床试验时颈椎与胸腰椎病患可以入组于同一临床试验,但对产品的应用会产生较大的约束(详见后述“脊椎节段比例”部分的分析)。
影像学终点为主要评价指标的临床试验,通常会考虑使用独立的中央影像学评价中心,以此来减小评价中的偏倚。
(2)次要评价指标
脊柱功能评分与围手术期处理、术中操作及术后康复训练等临床治疗的综合因素相关,其评价内容并非针对所申报融合器与同品种已上市产品的差异之处,亦非单纯针对融合器应发挥的作用,混杂因素较多,故而应作为次要评价指标。当然,若临床前研究所确定的风险盲点无法仅通过单纯的椎间融合状况来评价,就可能考虑将综合的疗效评价量表纳入主要评价指标的联合终点中。例如某些新材料融合器,若必需通过融合节段附近及全身的免疫反应来评价与人体的相容性时,对病患的脊柱功能评价就应成为主要评价指标的要素之一。
JOA评分、Oswestry功能丧失指数ODI、NDI、ODOM量表、VAS量表、SF-36调查问卷等均为临床诊治中常用的功能评价表,在使用中不仅应记录治疗前后的分值,还应计算改善率,例如JOA评分的改善率计算公式:
JOA评分改善率=(术后分-术前分)/(总分-术前分)×100%
各类评价表的运用对于控制临床试验中入组病例的基线是很有意义的。
(3)安全性评价指标
除了融合器相关不良事件如融合器移位、沉陷等等失效事件,椎间隙高度丢失率的计算也同样应进行记录。不良事件及继发干预相关的信息都是记录的重点,尤其严重不良事件。
不良事件是临床数据中的重点内容,尤其严重不良事件。严重不良事件,是指临床试验过程中发生的导致:死亡;病人、使用者或者他人健康严重恶化,包括:致命的疾病或者伤害、身体结构或者身体功能的永久性缺陷、需住院治疗或者延长住院时间、需要进行医疗或者手术介入以避免对身体结构或者身体功能造成永久性缺陷;导致胎儿窘迫、胎儿死亡或者先天性异常/先天缺损等事件。
临床试验过程中的全部不良事件均应报告,并对不良事件发生率做出整体评价,应按照与器械的相关度进行分层分析,例如:从神经/功能/疼痛等并发症的术前/术中/术后与器械/手术部位/全身系统的关系进行分层。同时有多项不良事件发生的病例应着重描述。其中,与产品操作使用(而非产品失效)相关的不良事件会较多,且不同医疗地区所上报的情况会有所不同。各分层数据的原因分析中,要注意产品及植入操作本身对人体的作用模式本身会否产生数据评价中的不良事件,例如由于融合器存在而引起的疼痛、不适或感觉异常,由于手术操作引起的软组织或血管损伤,因神经根或硬膜的过度撑开牵引或损伤而导致的神经并发症(Horner综合征、迷走神经损伤等)、脑脊液漏、术后颈肩痛、腰背肌损伤所致的术后难治性腰背痛、吞咽或呼吸困难、临近节段退变等。这些不良事件应与由于融合器安全性较差而产生的不良事件相区别,如融合器下沉、松动、移位、脱落、碎裂,椎体骨折、骨裂、骨吸收、骨不连以及由之引发的神经压迫症状(包括疼痛、麻痹等)和病理体征,另外也应明示植入后诱发的过敏反应、局部肿瘤等不良反应。若不良事件体现出产品风险分析中未纳入分析防控的危害,应着重进行阐述,包括采取的改进措施如设计修改、植入操作改进或适应证(如具体的椎体滑脱Meyerding分型等)、禁忌证及注意事项的进一步细化。
在不良事件中,继发的外科干预要独立做多元化的分析。这些外科干预包含翻修(包括去除、替换和重置融合器或组件)、移除融合器但不替换新产品而选择其他融合方式、再手术(如进一步解压操作)和补充植入其他固定物,等等。
3. 样本量设定
针对主要评价指标和临床历史数据,进行高质量数据分析和计算,确定试验组主要评价指标的预期有效率,结合所设定的统计学类型之后,方能合理设定样本量。样本量的计算公式及计算结果有诸多的统计学文献可供直接查询,例如历史数据支持的联合终点有效率(优良率)为95%,双侧检验α取0.05,β取0.1,非劣效界值δ取0.15时,每组病例数为45例,一般考虑10%脱落率后每组入组病例数为50例,其他参数不变而δ取0.1时每组入组病例数为111例;单组目标值试验时,双侧检验下若经文献等历史数据统计后的目标值设定为85%,β取0.2时,一般考虑10%脱落率后入组病例数为87例。这里要注意,较少的样本量通常情况下需要较多高质量文献数据集对各项参数取值进行支持,这在一定程度上也会增加申请人的负担。例如单侧检验、非劣效检验中预期有效率提高、目标值降低、β扩大及δ扩大均会降低样本量,但必须经统计处理的、充分分析的文献数据支持。
4. 入排标准和脊椎节段比例
入排标准及病例结构关系到主要评价指标的观察是否建立在均衡的基线上,对于试验质量及试验结果对所宣称功效的支持力度很重要。
(1)入选标准
椎间融合器临床试验入选病例时首先应注意年龄和性别的分布,这两项因素关系到患者骨质代谢状况,从而影响着试验的均一性。鉴于脊柱融合术一般用于骨骼发育成熟患者,建议入组患者年龄>18岁并具有较集中的分布。中老年男性与女性在病因及骨代谢特点上有一定的统计学差别,因而建议试验组与对照组的组内男女病患比例相一致。
入组病例治疗所涉及的脊柱节段应明示,如颈椎及胸腰椎的具体位置。尤其对于多节段治疗的患者,应将各节段的疾病信息表述清晰,这对入组病例基线均衡性的分析至关重要。
与主要评价指标相适应,病患节段的疾病信息主要包括影像学上判定的脊柱失稳的病理类型(如创伤还是退行性变引起的、脊髓型还是神经根型的脊椎病)、疾病分级分期分型(如脊柱滑脱的Meyerding分型、椎间盘退变的病理分型)等等,尤其对于特殊设计的椎间融合器产品。
与临床实践相符的是,入组患者一般都经历了至少4—6周的不成功的非手术保守治疗。
按照常规临床试验“意向性试验”的基本要求,入组患者必须是自愿参加试验,能够准确理解并签署知情同意书,能够遵守术后管理程序,能够配合试验计划完成术后随访。
(2) 排除标准
排除标准的内容不仅仅关系到入组患者的基线均衡性、整体试验的质量及试验结果的意义,还关系到入组患者的安全性。以下是脊柱临床试验普遍的排除标准,常常与最终的禁忌症有一定相关性:
a)明显的局部或全身严重感染,如骨髓炎;
b)可能导致术后护理期间出现难以接受的固定失败或并发症风险的任何精神或神经肌肉及血管疾患;
c)妊娠;
d)手术部位没有足够软组织覆盖的患者;
e)明确的或怀疑对产品所用金属、高分子材料或对异物过敏;
f)骨质疏松症、骨软化症或类似的骨密度降低是手术的相对禁忌症,因为他们可能会降低已达到的校正程度和/或机械固定的效果,尤其是对于高龄严重骨质疏松症患者;
g)系统性或代谢性疾病;
h)患者的总体健康状况不良,如冠心病、高血压等常规全麻手术禁忌症;
i)会导致植入物固定失败或者植入物本身因负荷过重而损坏的肥胖症;
j)患者不愿意或无能力遵循术后疗法和/或康复方案的指示;
k)精神疾病、药物滥用或酗酒;不能保证在骨折愈合期间戒烟患者;
l)由于疾病、感染或以往的手术操作而影响现存骨量,使之不能给植入装置提供足够的支撑和/或固定,并影响骨性融合;
m)脊柱肿瘤,包括转移瘤;
n)长期服用影响骨、软组织愈合的药物(如化疗药物、皮质类固醇激素,除外甲泼尼龙);
o)正在接受放射治疗者;
p)使用生长因子,长期使用镇静催眠药(连续使用3个月以上),长期使用非甾体类消炎药(连续使用3个月以上);
q)研究者判断不适合入选的其他情况(如:小儿麻痹后遗症等)等;
r)患者精神上无能力或者不能理解参与研究的要求;
s)预计无依从性;
t)骨骼不成熟,正在发育中的患者;
u)受试者合并的其他疾病限制其参加研究,不能依从随访或影响研究的科学性完整性;
v)拒绝签署知情同意书者。
需明确指出的是,未纳入临床试验与不列入产品适应证是两个概念。研究者需要将试验所验证的适应证扩展到对最终宣称的适应证的支持,此部分分析论证也包括前述假关节病患及既往融合失败病患。通常外推出的适应证需要明确更多的注意事项及限制条件。
(3)脊椎节段比例
椎间融合器通常与脊柱内固定系统联合使用,脊柱内固定系统已可提供坚强的脊柱初始稳定性,这就使得辅助脊柱内固定的情况下,颈椎间和胸腰椎间的局部融合环境及对椎间融合器融合效果的影像学观察指标趋于同质化,临床试验中主要评价内容就集中为评价椎间融合器促进椎间骨性融合的能力。因此联合脊柱内固定的椎间融合器的病例,不论术式、手术入路或应用部位,在评价椎间骨性融合效果上具有同质性,可以招募入同一组进行试验并统一进行统计分析。
鉴于其他次要评价指标及安全性评价指标的需要,试验组与对照组间应有可比性,建议各组内均包含颈椎或胸腰椎病例,例如均不少于该组病例总数的1/3。
然而,颈胸腰椎入组的同质性是有严格前提的,即:直至随访时间终点,所治疗的病患节段的内固定系统仍未取出。这貌似减少了临床试验的成本,但对融合器的长期风险评价及使用方法会产生极大限制,例如,若产品宣称在一定时间后或一定情况下可移除内固定,则随访观察节点应包括取出内固定后椎间融合效果的观察,此时由于颈椎段与胸腰椎段脊柱的生理活动度差异,颈椎与胸腰椎融合的动力位X线平片的判定标准在椎间平移运动度及成角运动度方面有差异,故而可能造成颈椎与胸腰椎病例的异质性,最终需要分别进行临床试验或补充已有的临床试验。如果融合时的平移运动度及成角运动度的衡量能够统一,例如统一取脊柱融合判定的最严格标准即平移运动=0mm、成角运动<2°,则颈胸腰椎原则上仍可招募在同一试验内。但此时应注意,这可能使更多病例被判定为不融合,尤其对于生理活动度本身很大的颈椎部位的融合术,临床试验结果将可能不支持受试产品的安全有效。
5. 随访窗口及试验持续时间
为全面客观地体现入组病患的椎间融合效果,一般来讲椎间融合术后需经历6—12个月的随访期。缩短试验时间将可能仅仅观察到内固定辅助环境下的椎间活动度,对远期去除脊柱内固定后椎间融合效果的支持力度较弱。
每例病患的随访时间点至少包括术前、术后1周内、术后3月±2周、术后6月±2周,若方案中设定随访期为9或12个月,应相应包括术后9月±1月及术后12月±1月,鼓励根据患者安全性数据的表现相应地增加随访窗口数量并缩短各窗口期的跨度。
6. 数据呈现
各入组病例的信息清单中,患者术前及术后诊断结果(包括受累节段和疾病类别等)、所使用器械的型号规格数量等信息应详尽。临床试验过程中所有来源于CRF的随访信息均应列表汇总,而非笼统地描述。注意应按组别而非个体病患汇总各随访时间窗的各项观察终点的信息,例如术后3月±2周时试验组达到“优”级融合的比率及融合器移位率,术后6月±2周时对照组达到“优”级融合的比率及融合器移位率。这里“率”的呈现应以“达标病例数/随访病例数×100% =比率”的方式在数据表格中给出,例如“10/50×100%=20%”。建议各随访时点的各观察终点信息应并列呈现在同一表格内。含有多个融合节段的病例应将各节段中最差表现作为该病例观察终点的信息。
对未遵守临床试验方案的病例应单独呈现,并最终分析这些病例对整体试验结果的统计学影响。
不良事件应按各随访时间点及各观察终点全面客观呈现,与前述“安全性评价指标”内容一致,应分层为器械、手术和全身系统相关的不良事件,并进行原因分析。术后的翻修、移除、再手术、补充固定及其他继发外科干预事件要独立于其他不良事件,单独进行呈现。“翻修”可包含去除、替代和重置一个组件,“移除”可能带有替换,“再手术”不包括移除、修正、替换或增加植入器械,“其他外科干预”是与所研究融合器无关的外科手术。值得注意的是继发外科干预事件的病例应与死亡等严重不良事件病例一同纳入失败病例。
7. 统计分析
人口统计学与基线特征方面,除了骨科医疗器械临床试验常见的共性信息,如性别、年龄、体重、骨质情况、既往病史、手术史(尤其脊柱手术)及伴随的内科疾病情况等,研究者还应对试验干预脊柱节段的病情基线(如各类评价表得分)进行分析,具体方面与入选标准中考虑的因素相一致。最终的分析结果应对入选病例基线不均衡之处,以及对试验偏倚的影响进行论证,必要时可考虑协方差分析等方法进行基线分析。对多中心效应、非随机化设计等带来的试验偏倚,可通过倾向评分法(包括变量调整法、分层分析法及配比法)和回归分析等统计方法进行控制。
数据分析时应考虑数据的完整性,受试产品及受试者数据的剔除条件或偏倚数据的处理必须在统计方案中预先界定并给出依据。
对于涉及多节段融合治疗的病例,应对试验结果进行灵敏度分析,以患者为单位和以植入融合器为单位分别进行统计分析并比较。
临床试验的数据分析应基于不同的分析集,通常包括全分析集、符合方案集和安全分析集,研究方案中应明确各分析集的定义。全分析集中脱落病例主要评价指标缺失值的填补方法(如最差值法等)应在临床试验方案中予以事先明确,并进行灵敏度分析,以评价缺失数据对研究结果稳定性的影响。主要评价指标的分析应同时在全分析集和符合方案集上进行;安全性指标的分析应基于安全分析集。
对于主要评价指标,统计结果需采用点估计及相应的95%可信区间进行分析与评价。对于非劣效检验,主要评价指标的组间差值必须与非劣效界值有统计学意义上的差异,并且其差异的95%可信区间下限须大于-δ(以影像学稳定性的优良率为主要评价指标时),若以假体的影像学移位率为主要评价指标则组间差值的95%可信区间下限须小于δ,此时方能使假设检验的备择假设H1成立,从而判定试验器械非劣于对照组产品。
统计方案中应预先明确具体的统计分析方法(例如平衡基线的协方差、分析多中心效应的CMH、贝叶斯模型中马尔科夫链蒙特卡洛法等统计方法)、统计分析软件及其版本和相关计算过程中参数的设定,例如EpiData3.0、SAS9.4、SPSS19.0、WinBUGS14等软件及参数。
统计分析报告应纳入最终的临床试验总结报告中,各中心的数据应统一进行报告。
(八)延续注册时产品分析报告
延续注册时产品在注册证有效期内的产品分析报告应重点关注“(七)产品的临床试验”中第2条(3)中所述的融合器相关不良事件的审查要点。
(九)产品说明书、标签和包装标识
产品说明书、标签和包装标识应符合国家食品药品监督管理总局发布的《医疗器械说明书和标签管理规定》要求,还应符合相关国家标准、行业标准的要求,例如YY/T 0466.1《用于医疗器械标签、标记和提供信息的符号》。
产品临床适用范围/适应证、禁忌症、并发症、注意事项应与临床试验所验证的范围一致,例如适用范围“适用于进行脊柱融合术时支撑椎体,提供即刻稳定性,支持正常的骨性融合过程。明确适用部位为颈椎(Cx—Cx)或胸腰骶椎(Tx—Lx/S1)。通常与内固定装置配合使用于脊柱节段退行性失稳、脊柱节段创伤性失稳、脊椎滑脱、椎间减压术后(脊柱节段医源性失稳)、脊柱侧凸矫正”,禁忌症包括临床试验方案中的排除标准内容;并发症和警告内容提示“骨不连(假关节形成)或延迟愈合;感染、无菌性炎症;由于植入物存在而引起的疼痛、不适或感觉异常;由于手术操作引起的神经、软组织或血管损伤;由于应力遮挡导致的骨密度降低及骨吸收;骨折及骨裂;因神经根或硬膜的过度撑开牵引或损伤而导致的神经并发症;对植入物的过敏反应;植入物下沉、椎间隙高度的降低;植入物松动、移位、脱落、碎裂;邻近节段退变;异位骨化;难治性颈、胸、腰痛综合症;椎旁韧带肌肉组织损伤”,等等内容。
作为脊柱内植入物,椎间融合器的MR兼容性很重要。鼓励企业按照ASTM F2182、F2052、F2119对核磁环境下椎间融合器的致热、位移及伪影进行测试与评估,并相应地在说明书中明确植入后临床核磁检查的限制条件,作为警示或注意事项内容的一部分。
产品有效期、植入后从人体取出的条件、采用的灭菌方法、非灭菌产品推荐采用的灭菌方法等信息应与产品研究资料所述一致。
四、参考资料
1. 《医疗器械监督管理条例》(中华人民共和国国务院令第650号)
2. 《医疗器械注册管理办法》(国家食品药品监督管理总局令第4号)
3. 《医疗器械临床试验质量管理规范》(国家食品药品监督管理总局令第25号)
4. 《医疗器械说明书和标签管理规定》(国家食品药品监督管理总局令第6号)
5. 《医疗器械临床评价技术指导原则》(国家食品药品监督管理总局通告2015年第14号)
6. 《关于公布医疗器械注册申报资料要求和批准证明文件格式的公告》(国家食品药品监督管理总局公告2014年第43号)
7. YY/T 0316《医疗器械 风险管理对医疗器械的应用》
8. 《无源植入性医疗器械产品注册申报资料指导原则》(食药监办械函〔2009〕519号)
9. 《无源植入性医疗器械货架寿命申报资料指导原则》(食药监办械函〔2011〕116号)
五、指导原则编写单位
国家食品药品监督管理总局医疗器械技术审评中心。
附录
椎间融合器产品风险管理资料要求
一、总体要求
申请人应提供产品上市前对其风险管理活动进行全面评审所形成的风险管理报告以及相关的产品风险管理资料。该风险管理报告应说明:(1)风险管理计划已被适当地实施;(2)综合剩余风险是可接受的;(3)已有恰当的方法获得与本产品相关和出厂后流通与临床应用的信息。
除此之外,风险管理报告还应扼要说明:(1)在产品研制的初期阶段,对风险管理活动的策划及所形成的风险管理计划;(2)说明已识别了产品有关的可能危害,并对其危害产生的风险进行了估计和评价;(3)在降低风险措施方面,考虑了相关安全标准和相关产品标准,并有针对性地实施了降低风险的技术和管理方面的措施;(4)通过产品的成分、性能等测试、生产的基本工艺的确认及验证、相关文件的审查、试生产等活动对风险控制措施的有效性实施验证;(5)应对产品的安全性做出承诺。
风险管理报告应由最高管理者(法人)或其授权的代表签字批准。
二、风险管理报告及风险管理资料内容
1. 职责权限
应明确参与风险管理活动的成员,包括风险分析人员、风险评价人员、风险控制措施制定人员及验证人员、风险管理过程评审人员以及风险管理报告的编制及审批人员,他们可能是同一组人,应列出其姓名、职务及责任范围。其成员应具有与风险管理任务相适应的知识和经验。
2. 产品描述
(1)通过照片、结构图、图表和文字描述等形式表征产品的型号规格、组件以及关键部位;
(2)各组件的材料牌号;
(3)各型号产品的具体适用部位(如颈椎、胸椎、腰椎等);
(4)生产工艺流程;
(5)适用的国家标准、行业标准、国际标准。
3. 产品的安全特征判定
应按照YY/T 0316《医疗器械 风险管理对医疗器械的应用》附录C提示的问题,针对实际情况对产品的安全特征作简明描述。产品如存在附录C提示以外的可能影响安全特征的情况,也应做出说明。最终形成一份《产品安全特征清单》。
4. 产品的可能危害判定
应在《产品安全特征清单》的基础上,系统地判定产品在正常和故障两种条件下的可预见危害。并对危害的成因及后果做多元化的分析,即说明危害、可预见事件序列、危害处境和可能发生的损害之间的关系。形成一份产品可预见的危害及危害分析清单。
5. 对危害清单中每一危害处境下的风险进行风险估计和风险评价
应明确风险可接受准则,并对损害发生的概率和损害的严重程度予以明确定义;产品国家标准、行业标准中如涉及了相关风险的可接受准则,该准则应作为申请人所确定的风险可接受准则之一,除非有证据证实其特定风险的可接受准则不必符合相关标准。应依据风险可接受准则对危害清单中每一危害处境下的风险进行风险估计和风险评价。
风险评价的结果可以记入《风险评价、风险控制措施以及剩余风险评价汇总表》中。
6. 降低风险的控制措施
应对经风险评价后不可接受的或考虑可进一步采取措施降低的风险实施降低风险的控制措施。在制定降低风险的控制措施方案时,应充分考虑产品国家标准、行业标准中有关降低风险的措施。应确保降低风险的控制措施在研制初期得到有效的输入,并应对措施的有效性实施验证。
7. 应对采取降低风险的控制措施后的剩余风险以及是否会引发新的风险进行评价。
以上降低风险的控制措施、控制措施的验证、剩余风险评价等信息可以记入《风险评价、风险控制措施以及剩余风险评价汇总表》中。
8. 结论
应对综合剩余风险是否可接受给出结论性意见,并对已有恰当的方法获得与本产品相关和出厂后流通与临床应用的信息进行阐述并做出承诺。
责任编辑:









